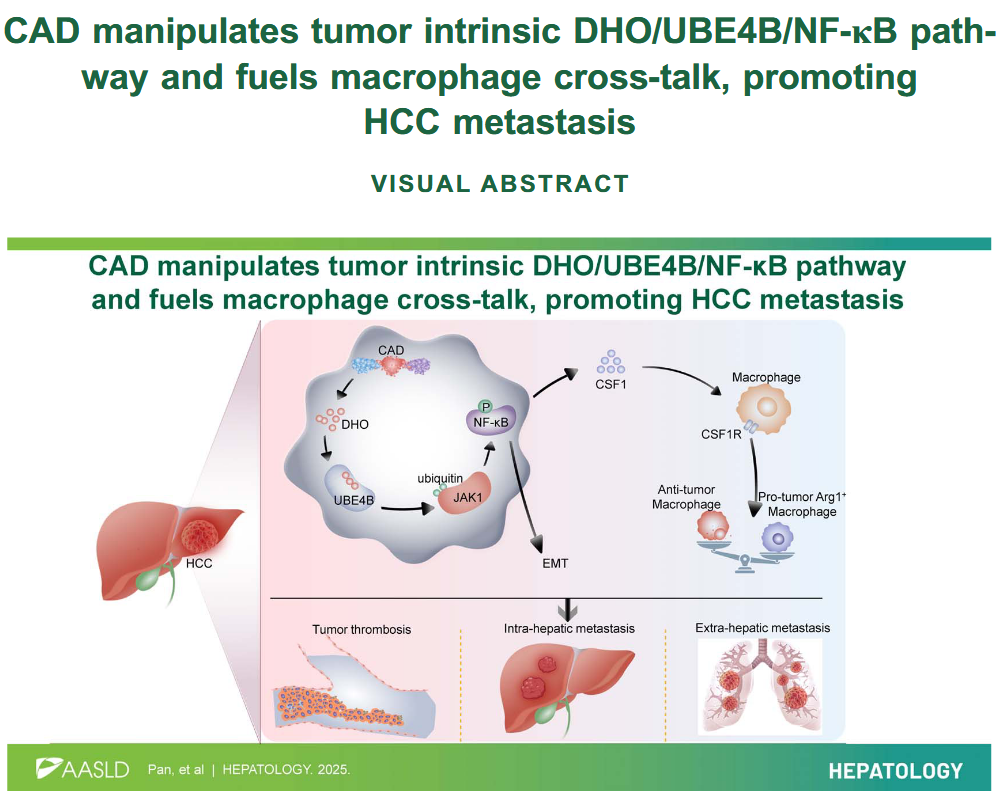
2025年2月,复旦大学附属中山医院的研究团队在《Hepatology》发表了题为《CAD manipulates tumor intrinsic DHO/UBE4B/NF-κB pathway and fuels macrophage cross-talk, promoting HCC metastasis》的研究,系统解析了嘧啶代谢关键酶CAD在肝细胞癌转移及门静脉癌栓形成中的关键作用。本研究结合多组学分析、代谢示踪及体内外功能实验,对比分析了伴随与不伴随门静脉癌栓的HCC样本,明确发现CAD在高转移性HCC中显著上调,并与侵袭性表型密切相关。在机制研究中,作者创新性地引入SPIDER技术,成功捕获了代谢产物二氢乳清酸(DHO)与泛素连接酶UBE4B之间的直接相互作用,揭示了DHO–UBE4B–JAK1–NF-κB这一此前未知的非经典信号通路。进一步研究表明,该通路一方面诱导肿瘤细胞上皮—间质转化,增强迁移和侵袭能力;另一方面通过促进CSF1分泌,驱动肿瘤相关巨噬细胞向免疫抑制型表型极化,从而协同促进肝癌转移和门静脉内定植。在治疗验证层面,CAD抑制及CSF1R靶向干预在小鼠模型中显著抑制肿瘤进展,提示CAD及其下游信号轴具有明确的转化医学潜力。该研究不仅拓展了人们对肿瘤代谢功能的传统认知,也充分展示了SPIDER技术在解析代谢物—蛋白互作及复杂疾病机制中的独特优势。
研究背景
肝细胞癌(Hepatocellular carcinoma,HCC)是一种高度侵袭性的消化系统恶性肿瘤,其高死亡率主要源于早期缺乏特异性症状以及极强的转移能力。其中,门静脉癌栓(portal vein tumor thrombus,PVTT)是HCC最常见、也是最具挑战性的转移形式之一,显著限制了外科手术及系统治疗的临床获益。长期以来,研究者普遍将肿瘤转移归因于基因突变、信号通路异常及肿瘤微环境改变,而肿瘤代谢更多被视为支持肿瘤增殖的“背景因素”。然而,在临床实践中,即便在分期、病理特征相似的HCC患者中,PVTT的发生风险仍存在显著差异,提示其背后可能潜藏着尚未被充分认识的分子调控机制。受限于传统研究手段,代谢中间产物如何直接参与信号转导、并在肿瘤转移和免疫重塑中发挥作用,长期缺乏系统性证据。
技术路线
1、 核心靶标筛选:多组学数据分析锁定CAD
2、 CAD功能验证:体内外实验确认促转移作用
3、 双重调控机制解析
机制解析(一):肿瘤细胞内在通路:DHO/UBE4B/JAK1/NF-κB
机制解析(二):肿瘤微环境(TME)重塑:CAD介导巨噬细胞重编程
4、 临床相关性与泛癌潜力验证
主要结果
本研究围绕肝细胞癌(HCC)转移及门静脉癌栓(PVTT)形成的核心机制,采用“靶标筛选-功能验证-机制解析-临床确证”的系统性技术路线,整合多组学分析、分子生物学、动物模型及临床样本验证等多维度技术手段,层层递进阐明CAD蛋白的调控作用及分子机制,具体如下:
1.多组学整合筛选HCC转移及PVTT形成的核心调控因子CAD
基于159例HCC患者(含37例PVTT阳性)的proteogenomics整合数据(基因组、转录组、蛋白组),通过GSEA算法对比PVTT阳性/阴性样本、肿瘤与癌旁组织的差异富集生物学过程,聚焦嘧啶代谢通路进行差异表达蛋白筛选,结合单因素及多因素Cox回归分析与生存分析,锁定嘧啶代谢关键酶CAD为驱动HCC转移及PVTT形成的核心调控因子,明确其独立预后价值(HR=1.98/1.90,p<0.001)。
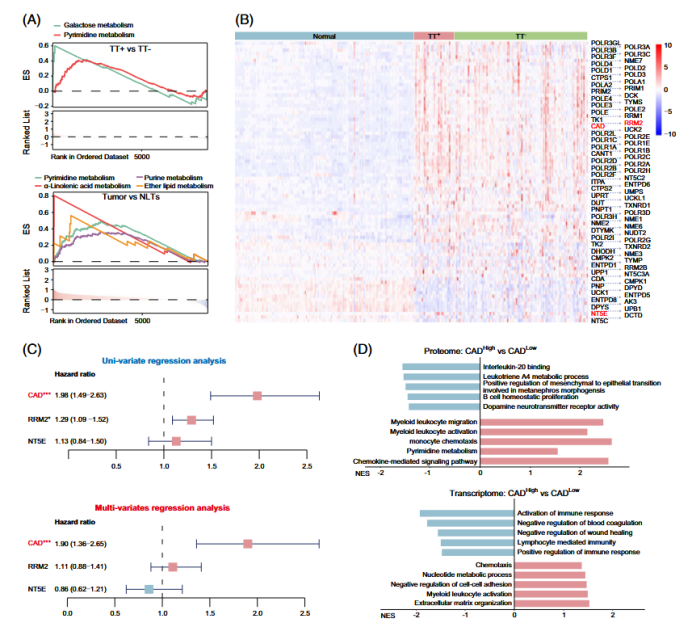
FIGURE1 Identification of CAD as the crucial contributor to HCC metastasis.
2.CAD促HCC转移的体内外功能验证
开展体内外功能验证以确认CAD的促转移效应:体外层面,选取高/低转移潜能HCC细胞系(MHCC97H、HCC-LM3、CSQT-2vsHepG2、Huh7),构建CAD过表达(Huh7)及敲低(HCC-LM3、CSQT-2)稳定细胞系,通过Transwell迁移/侵袭实验检测细胞转移能力,Western blot检测上皮间质转化(EMT)标志物表达,并利用CAD特异性抑制剂PALA干预验证效应特异性;体内层面,在裸鼠(HCC-LM3、Huh7)及C57BL/6小鼠(Hepa1-6)中构建皮下移植瘤及原位肝移植瘤模型,通过肿瘤移植、PALA药物干预及组织病理学分析,评估CAD对PVTT形成率、肝内及肺转移灶数量的影响,从细胞和动物水平双重证实CAD的促转移功能。
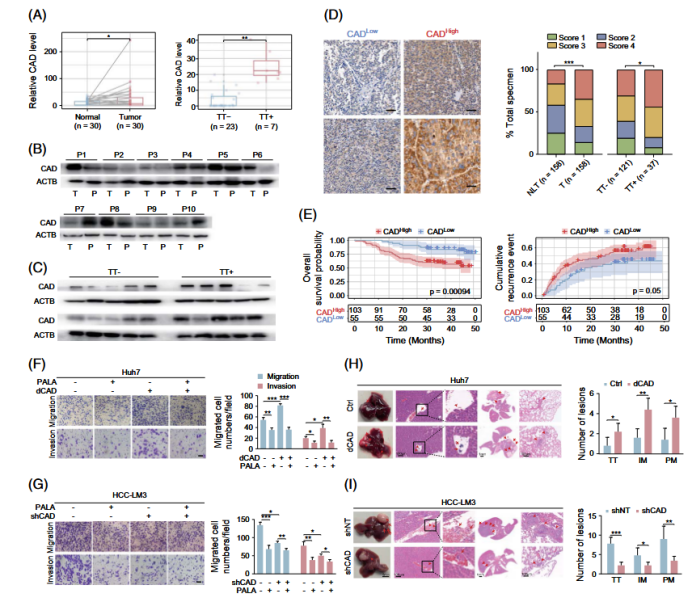
F I G U R E 2 CAD upregulated in HCC tumor tissues and associated with HCC invasive behavior.
3.肿瘤细胞内在调控机制解析:DHO/UBE4B/JAK1/NF-κB通路
针对肿瘤细胞内在通路,采用LC/MS代谢组学技术检测CAD过表达/敲低细胞的代谢谱差异,结合N15-谷氨酰胺同位素追踪技术动态追踪嘧啶从头合成代谢流向,筛选并验证二氢乳清酸(DHO)为介导CAD促转移的关键代谢产物;进一步通过合成生物素标记DHO探针,应用SPIDER技术(特异性普普化标记身份报告技术)富集细胞裂解液中与DHO直接结合的蛋白,经质谱分析筛选潜在靶点后,通过免疫沉淀(IP)实验确认泛素化因子UBE4B为唯一直接结合蛋白;再通过siRNA敲低UBE4B、体外泛素化实验、Westernblot检测JAK1泛素化水平及NF-κB通路激活标志物(p-P65、P65)与EMT标志物表达,结合NF-κB抑制剂(PDTC)、JAK1抑制剂(Itacitinib)干预验证,完整阐明“CAD→DHO积累→DHO结合UBE4B→促进JAK1泛素化→激活NF-κB通路→诱导EMT”的细胞内在调控通路。
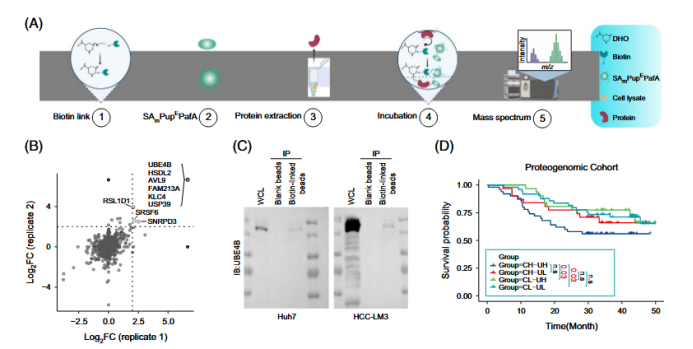
F I G U R E 4 DHO directly bound to UBE4B to promote NF-κB pathway and HCC metastasis.
4.肿瘤微环境重塑机制解析:CAD介导的巨噬细胞重编程
针对肿瘤微环境(TME)重塑机制,对CAD敲低及对照组HCC原位瘤组织进行单细胞RNA测序(scRNA-seq),鉴定TME中11类主要细胞类型,通过SCENIC转录调控分析明确肿瘤相关巨噬细胞(TAMs)的3种亚型(Arg1+促肿瘤型、Clec4f+抗瘤型、Dnase1l3+中间型)及其功能属性;构建HCC细胞与巨噬细胞共培养体系,结合转录组数据分析筛选CAD调控的关键细胞因子(CSF1),通过体外实验验证CAD对CSF1分泌的调控作用;体内采用ClodronateLiposomes(非特异性清除巨噬细胞)及PLX3397(CSF1R抑制剂,特异性清除Arg1+TAMs)干预C57BL/6小鼠原位瘤模型,明确CAD通过分泌CSF1诱导Dnase1l3+TAMs向Arg1+促肿瘤型极化,形成免疫抑制微环境的调控模式。
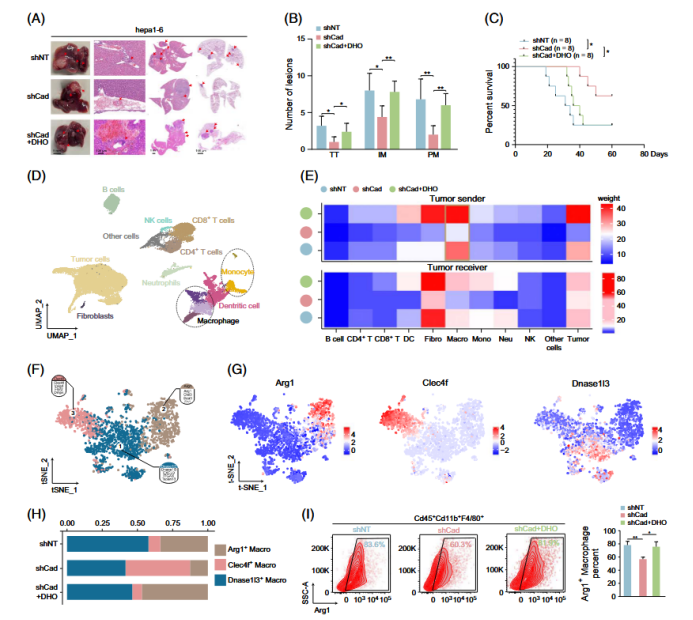
F I G U R E 5 CAD reprogrammed TME macrophage into “protumor” phenotype.
5.CAD的临床相关性与泛癌调控潜力验证
开展临床相关性验证以确证CAD的临床价值:采用qRT-PCR(30例样本)、Westernblot(10例样本)检测HCC肿瘤与癌旁组织中CAD的mRNA及蛋白表达水平,在2个独立HCC队列中通过免疫组化(IHC)分析CAD表达与BCLC分期、TNM分期、PVTT形成等临床病理参数及患者总生存期(OS)、无复发生存期(RFS)的关联;同时利用TCGA(24种癌症)、TCPA公共数据库,分析CAD在不同癌症类型中的肿瘤/正常组织表达差异、预后价值及与NF-κB通路激活的相关性,系统证实CAD的临床相关性及泛癌调控潜力。
研究总结
研究意义:为HCC治疗开辟双靶点新方向
·首次揭示CAD的双重促转移机制:既通过“DHO/UBE4B/JAK1/NF-κB通路”激活肿瘤细胞内在转移潜能,又通过“CSF1介导的巨噬细胞重编程”重塑免疫抑制微环境,二者协同推动HCC转移及PVTT形成;
·SPIDER技术的范式价值:为解析“代谢物-蛋白互作”提供了全新技术工具,破解了传统方法的技术瓶颈;
·明确临床转化潜力:靶向CAD不仅可直接抑制肿瘤细胞转移,还能逆转免疫抑制性TME,为HCC尤其是PVTT患者提供了全新治疗方向,也为泛癌治疗研究提供了新思路。
参考文献
Pan, Jiaomeng, Mao Zhang, Dongning Rao, et al. 2025. ‘CAD Manipulates Tumor Intrinsic DHO/UBE4B/NF-κB Pathway and Fuels Macrophage Cross-Talk, Promoting HCC Metastasis’. Hepatology, ahead of print, March 12. https://doi.org/10.1097/HEP.0000000000001304.
Wong, Carmen Chak-Lui, and Chun-Ming Wong. 2025. ‘CAD-Driven Pathways in HCC Metastasis’. Hepatology, ahead of print, March 18. https://doi.org/10.1097/HEP.0000000000001315.